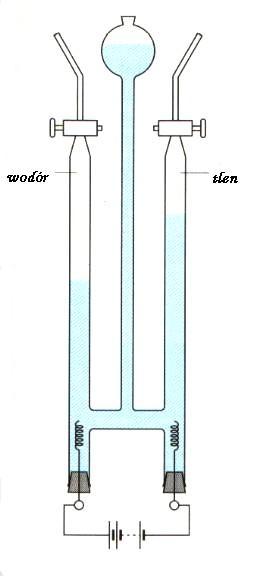
bądź w zestawach laboratoryjnych własnej konstrukcji:

Każde z tych urządzeń jest elektrolizerem, czyli układem składającym się z dwóch (jednakowych lub różnych) przewodników metalicznych (zwanych elektrodami), zanurzonych w roztworze przewodzącym prąd elektryczny (czyli w roztworze elektrolitu), co można przedstawić schematem:
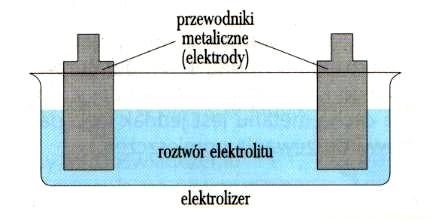
Elektrody mogą mieć formę blaszek, prętów lub drucików, mogą częściowo wystawać nad powierzchnię roztworu elektrolitu lub być w nim zanurzone w całości, ale rodzaj materiału, z którego są wykonane należy tak dobrać, aby nie reagował chemicznie z roztworem elektrolitu.
Czysta woda bardzo słabo przewodzi prąd elektryczny, ponieważ zawiera tylko niewielką ilość jonów H+ i OH- wytworzonych w procesie autodysocjacji. W konsekwencji uzyskanie widocznych ilości wodoru i tlenu trwałoby bardzo długo. Dlatego elektrolizie należy poddać wodny roztwór odpowiedniego elektrolitu. Należy przypomnieć, że elektrolit to substancja, której wodny roztwór przewodzi prąd elektryczny. Do elektrolitów należą rozpuszczalne w wodzie:
*sole
*wodorotlenki
*kwasy
Są to substancje ulegające dysocjacji jonowej i wytwarzające duże ilości jonów. Jednak nie każdy elektrolit nadaje się do przeprowadzenia elektrolizy wody, czyli rozkładu jej na wodór i tlen. Na przykład podczas elektrolizy wodnych roztworów zawierających kationy metali ciężkich na elektrodzie połączonej z ujemnym biegunem źródła prądu może wydzielać się metal, a nie wodór. Elektroliza wody nastąpi wówczas, gdy elektrolit będzie zawierał kationy metalu lekkiego i aniony kwasu tlenowego lub aniony OH-. Można więc użyć na przykład: Na2SO4, H2SO4, NaOH.
Elektroliza rozpocznie się po połączeniu metalicznych przewodników z biegunami źródła prądu stałego:
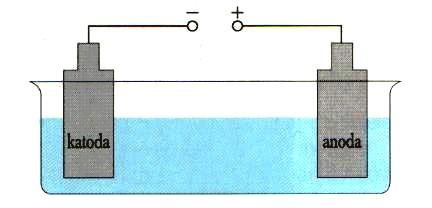
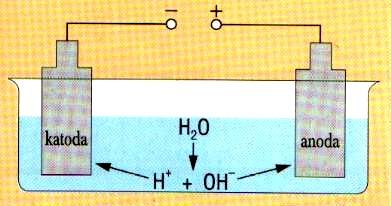
W tym momencie przewodniki metaliczne stają się elektrodami. Elektrodę elektrolizera połączoną z ujemnym biegunem źródła prądu nazywamy katodą. To na niej może wydzielać się wodór. Elektrodę elektrolizera połączoną z dodatnim biegunem źródła prądu nazywamy anodą. Na niej może wydzielać się tlen.
DOśWIADCZENIE
Aparat do elektrolizy napełnij roztworem elektrolitu. Jeżeli aparat jest wyposażony w elektrody platynowe, to można użyć 5- procentowych roztworów: Na2SO4, H2SO4 lub NaOH. Jeśli w aparacie elektrody są stalowe, to nie należy używać kwasu. Elektrody połącz ze źródłem prądu stałego, na przykład prostownikiem do ładowania akumulatorów. Elektrolizę prowadź przez około 15 minut. Porównaj objętości gazów zebranych nad elektrodami. Gaz którego objętość jest większa, wprowadź do probówki odwróconej dnem do góry i zbliż do niej łuczywo. Sprawdź również, jak zachowuje sie rozżarzone łuczywo w kontakcie z drugim gazem.
Gaz 1: wodór
Gaz 2: tlen
Jak prąd elektryczny rozkłada wodę?
Prąd elektryczny to ruch cząsteczek obdarzonych ładunkiem elektrycznym. W przewodnikach metalicznych poruszają się elektrony, a w roztworach elektrolitów- jony. Ujemnie naładowana katoda przyciąga do siebie jony dodatnie (kationy), a dodatnio naładowana anoda przyciąga jony ujemne (aniony).
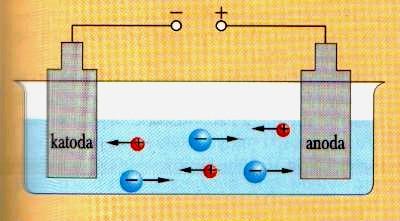
Po zderzeniu kationu z katodą jon ten przyłącza elektron lub elektrony, które stale do katody dopływają ze źródła prądu. Odwrotny proces zachodzi na powierzchni anody. Anion zderzający się z anodą oddaje jej elektron lub elektrony, a te przez obwód zewnętrzny podążają do źródła prądu. Rodzaj drobin powstających w tych procesach zależy od rodzaju jonów obecnych w roztworze.
Podczas tzw. elektrolizy wody, czyli procesu zachodzącego w elektrolizerze i dającego w końcowym efekcie dwa produkty: wodór na katodzie i tlen na anodzie, zachodzą liczne, wieloetapowe reakcje. Niżej przedstawiam ich uproszczoną wersję.
Każdy, nawet obojętny roztwór wodny, zawiera jony H+ i OH- pochodzące z autodysocjacji wody:
Źródło: Koluszek
