Wodór jest najpowszechniej występującym pierwiastkiem we Wszechświecie. Występuje w gwiazdach i obłokach międzygwiazdowych. Najprawdopodobniej jego atomy stanowią 91% wszystkich atomów wszechświata. Na Ziemi w stanie wolnym spotykany rzadko.
Jest to najprostszy pierwiastek składający się z jednego protonu i jednego elektronu. Wodór był więc p ierwszy! I tak na marginesie – jeśli wodór był pierwszy i niego powstawały następne pierwiastki, to najprawdopodobni ej też zawierał całą informację dotyczącą budowy pozostałych pierwiastków, Wszechświata i wszelkich jego el ementów – tj. także organizmów żywych. Mówi o tym teoria ingenezy Tadeusza Tellera, wg której ingeneza jest pierwotną informacją kodowaną układami superstrun w jądrach atomów. Treść ingenezy stanowi instrukcję-impera tyw nieustannego rozwoju organizmu Wszechświata i życia na Ziemi – w dodatku imperatyw zakładający piękno, doskonałość wszelkiego stworzenia.
ej też zawierał całą informację dotyczącą budowy pozostałych pierwiastków, Wszechświata i wszelkich jego el ementów – tj. także organizmów żywych. Mówi o tym teoria ingenezy Tadeusza Tellera, wg której ingeneza jest pierwotną informacją kodowaną układami superstrun w jądrach atomów. Treść ingenezy stanowi instrukcję-impera tyw nieustannego rozwoju organizmu Wszechświata i życia na Ziemi – w dodatku imperatyw zakładający piękno, doskonałość wszelkiego stworzenia.
Wodór ma symbol chemiczny „H” – od hydrogenium (łac., z gr. hydro – woda, genos – ród) „twor zący wodę”. Nazwa „hydrogenium” została nadana przez Antoine’a Lavoisier’a.
zący wodę”. Nazwa „hydrogenium” została nadana przez Antoine’a Lavoisier’a.
Pierwotnie polska nazwa była kalką łacińskiej – „wodoród” Używano także innych nazw: „wodor”, „lżeń”, „wod”, „wód” lecz z biegiem czasu została skrócona do powszechnie dziś znanej „wodór”. Jako pierwszy zaproponował tę nazwę Filip Neriusz Walter (1810-1847), wybitny polski chemik, za zasługi naukowe i pracę pedagogiczną odznaczony francuską Legią Honorową, specjalizujący się jako jeden z pierwszych w chemii organicznej, twórca polskiego nazewnictwa chemicznego. To Walter zaproponował polskie nazwy pierwiastków i wielu związków chemicznych. Przykładami są: azot, bar, bor, brom, cez, chlor, fluor, itr, jod, lit, magnez, osm, pallad, potas, rod, tellur, tor, wanad, węgiel, siarkowodór itd. (praca „Wykład nomenklatury chemicznej polskiej” - 1844).
Wodór jest gazem bezbarwnym, bezwonnym, a związki wodoru są najbardziej rozpowszechnionymi związkami na Ziemi. Wszelka materia biologiczna – od najprostszych składników cząsteczki DNA do złożonej struktury ludzkiej tkanki mózgowej – zawiera związki wodoru.

Prawdopodobnie pier wszą osobą, która opisała otrzymywanie wodoru w stanie czystym był szwajcarski alchemik i lekarz Phillippus Aureolus (1493-1541), występujący pod pseudonimem Theophrostus Bombastus von Hohenheim, znany pod przydomkiem Paracelsus. Przeprowadzał on eksperymenty polegające na wrzucaniu metali do kwasów i zbieraniu do naczyń gazowych produktów tych reakcji. Dziś taki sposób nadal stanowi najprostszy sposób otrzymywania tego pierwiastka w warunkach laboratoryjnych.
Pierwszą osobą, która uznała wodór za pierwiastek, był Henry Cavendish (1731-1810), człone k The Royal Society w Londynie, który w 1766 r. zamieścił w swoich notatkach tezę o uznaniu wodoru za pierwiastek. Substancja ta została uznana za pierwiastek ostatecznie jednak dopiero pod wpływem badań nad otrzymywaniem wody z wodoru i tlenu przez Antoine Lavoisier’a w 1783 r.
k The Royal Society w Londynie, który w 1766 r. zamieścił w swoich notatkach tezę o uznaniu wodoru za pierwiastek. Substancja ta została uznana za pierwiastek ostatecznie jednak dopiero pod wpływem badań nad otrzymywaniem wody z wodoru i tlenu przez Antoine Lavoisier’a w 1783 r.
Wodór tworzy trzy izotopy, z tego dwa stabilne. Zwykły wodór 11H posiada w jądrze atomowym tylko jeden proton, deuter 21H, inaczej D – posiada w jądrze oprócz protonu również jeden neutron oraz niestabilny tryt 31H zawiera jeden proton i dwa neutrony. Wodór zwykły (prot) występuje w postaci dwuatomowych cząsteczek H2, które rozpadają się w wysokich temperaturach na pojedyncze atomy. Zawartość deuteru w całej masie wodoru sięga 0,02%. Został odkryty w 1932 r. przez badawczy zespół amerykański pod przewodnictwem Harolda Claytona Urey’a, który za ten sukces otrzymał Nagrodę Nobla w 1934 r. Niestabilny, radioaktywny tryt wytwarza się sztucznie w wyniku przemian jądrowych, choć pow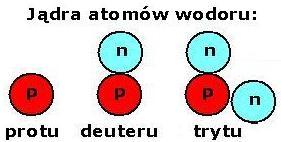 staje również w górnych warstwach atmosfery podczas bombardowań jąder azotu i tlenu przez promieniowanie neutronowe znajdujące się w spektrum kosmicznego promieniowania.
staje również w górnych warstwach atmosfery podczas bombardowań jąder azotu i tlenu przez promieniowanie neutronowe znajdujące się w spektrum kosmicznego promieniowania.
W warunkach laboratoryjnych naukowcy rosyjscy, francuscy i japońscy, po 40 latach badań, uzyskali również jeszcze jeden izotop wodoru – tzw. „wodór 5” – z protonem i czterema neutronami. Przypuszcza się, że ten typ wodoru powstaje we wnętrzu gwiazd pod wpływem niezwykle wysokich ciśnień i temperatur.
Dwa pierwiastki – wodór i tlen – tworzą tlenek wody H2O, czyli zwyczajną i jednocześnie niezwykłą (jeśli chodzi o własności) wodę, która zbudowana jest z cząsteczek składających się z jednego atomu tlenu i dwóch atomów wodoru. 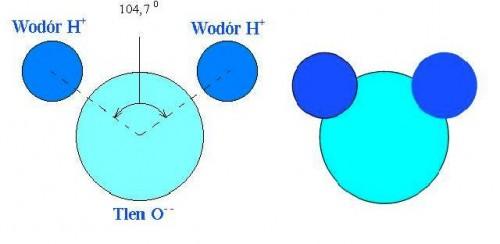 Zwykła woda jest podstawą wszelkiego życia i bogactwem przyrody.
Zwykła woda jest podstawą wszelkiego życia i bogactwem przyrody.
Okazuje się, że istnieją i inne rodzaje wód. W 1932 r. odkryto, że oprócz tzw. zwykłej wody istnieje i „ciężka” woda, w skład której wchodzi deuter – Н22О16 (D2О), zaś w 1951 r. otrzymano „superciężką” wodę, w skład której wchodzi tryt – Н32О16 (Т2О). „Ciężka woda” ma zdolność spowalniania neutronów (jest tzw. moderatorem w reaktorach atomowych).
W przyrodzie deuter istnieje w niewielkich ilościach, ale okazuje się, może również istnieć w organizmie ludzkim. Tworzy wodę „martwą” – działającą destrukcyjnie i trudno usuwalną. Im mniejsza jest zawartość "ciężkiej wody" w wodzie pitnej, tym wolniejszy jest podział komórek i zmniejsza się ryzyko podziałów nieprawidłowych oraz tym wolniej przebiegają procesy starzenia. Mimo niewielkiego stężenia w ludzkim organizmie (ok. 12÷14mmol/litr), to jej masa jest większa w porównaniu z np. masą wapnia czy masą magnezu – masa wody w organizmie wynosi przecież ok. 75÷80% masy ciała.
„Ciężka woda” może stać się dla ludzkości ogromnym rezerwuarem energii. Z jednego grama deuteru uzyskuje się energię dziesięć milionów razy większą niż z 1 grama węgla i 8 razy większą niż z toru stosowanego w elektrowniach atomowych. Deuter występuje w wodach mórz i oceanów w ilości 30 gramów deuteru na metr sześcienny wody. Sam deuter występujący w jeziorze wielkości Jeziora Genewskiego mógłby zapewnić zaopatrzenie ludzkości w energię na przeciąg kilku tysięcy lat. Zawartość deuteru w oceanicznych wodach szacuje się zaś na ok. 1015 ton (czyli milion miliardów).
Gdyby skonstruować reaktor termojądrowy o mocy termicznej ok. 820 GW (gigawatów) – 820 miliardów watów, pracujący na paliwie w postaci deuteru, to zużywałby on ok. 1 gram deuteru na sekundę (3,6 kg na godzinę, 86,4 kg na dobę). Dla porównania – w 2004 r. moc zainstalowana w reaktorach Unii Europejskiej wynosiła 136,6GW (przeciętna moc bloków energetycznych budowanych obecnie reaktorów to ok. 1500MW – 1500 milionów watów)…
„Jeżeli cała energia konsumowana przez ludzkość byłaby wytwarzana w procesie syntezy termojądrowej, ziemskie zasoby litu wystarczyłyby na 1000 lat. Wody do produkcji deuteru starczyłoby na wiele milionów lat. Jedna osoba żyjąca w kraju uprzemysłowionym zużyłaby przez całe swoje życie 30 gramów litu i 10 gramów deuteru.” („Sztuczne Słońce we Francji”, Rzeczpospolita, 9.06.2005 r.).
